酶聯免疫吸附分析 (enzyme-linked immunosorbent assay, ELISA)
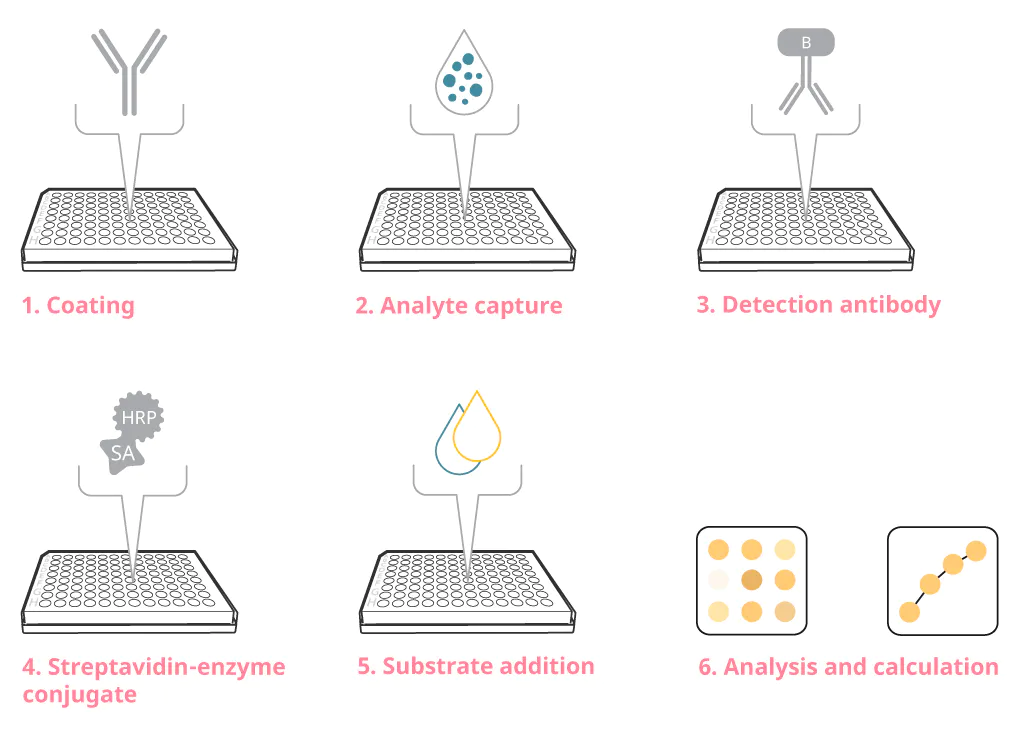
ELISA免疫分析試驗最初於1970年代開始發展,現今為實驗室及臨床診斷常用的檢驗技術之一。技術原理簡述由分析盤上的特異性單株抗體 (mAb)捕獲目標蛋白,再由另一支成對的單株抗體偵測並進行酵素呈色,最終藉由標準曲線進行絕對定量。
▲ELISA實驗流程示意圖。(1) 96孔盤上披覆Capture Ab (2) 加入待測樣品 (3) 加入與步驟1成對的Detection Ab (4) 加入酵素 (5) 加入受質 (6) 分析與定量
臨床檢體中的干擾因子
可能存在樣品中的干擾因子會影響抗體抗原的專一性結合,最終造成偽陽性 (false positive)結果。
干擾因子主要可分為以下兩種:
| 嗜異性抗體 (heterophile antibody) | ||
泛指能與二種以上不同來源的抗原作用的抗體,常見人類樣品中的「抗動物免疫球蛋白」抗體 (human anti-animal immunoglobulin antibodies, HAIA) 即為其一,例如人抗鼠抗體 (human anti-mouse antibodies, HAMA)。 此類抗體具有高度親和力及結合力,誘發來源可能為接觸動物產品、接受抗體免疫治療、受病原體感染或自體免疫疾病等 [1] | ||
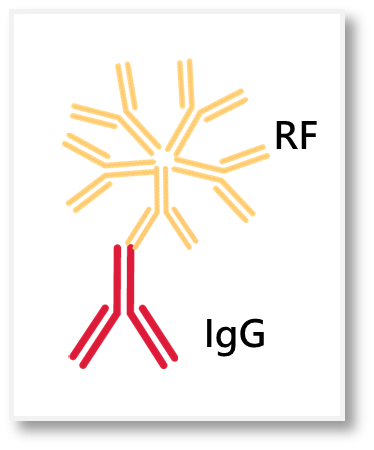
| 類風溼因子 (rheumatoid factor, RF) | ||
為一種自體抗體,最早是在類風濕關節炎患者身上發現,主要以IgM的形式存在。 廣義來說,RF也是一種嗜異性抗體,可與自身體內的免疫球蛋白IgG的Fc結合,進而引發可能造成組織器官損害的免疫反應 [1]。 |
干擾因子如何影響ELISA結果
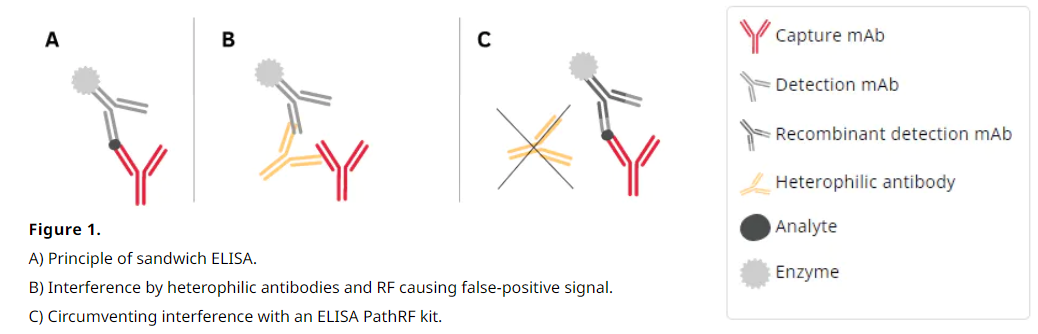
| 常規ELISA分析 |  | 正確的ELISA分析是藉成對抗體 (Capture Ab & Detection Ab)與分析物的專一性結合後,再行酵素反應呈色分析。 | 真實訊號 |
| 存在干擾因子 |  | 若檢體中存在會與其它抗體進行非特異性結合的干擾因子,則干擾因子與ELISA成對抗體交互作用,最終出現偽陽性結果。 | 偽陽性結果 |
RF因子並非類風濕關節炎患者的專利
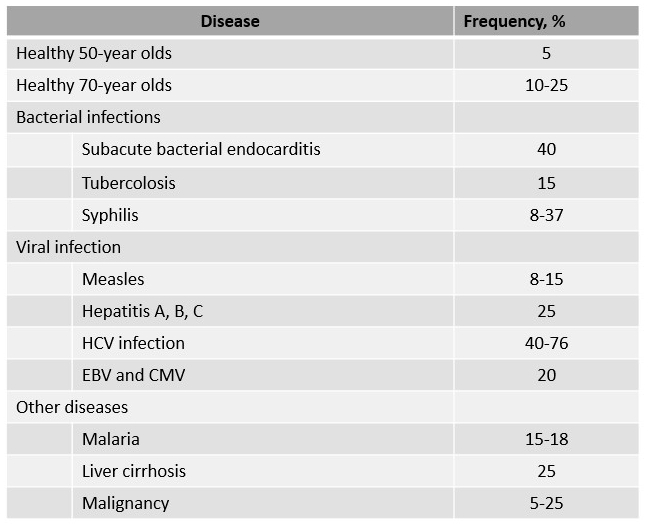
除了可在類風溼關節炎患者中檢測出RF陽性 (約7到9成);其他自體免疫疾病患者,例如:乾癬、紅斑性狼瘡、全身性硬化症等;細菌、病毒、寄生蟲感染或慢性疾病、吸菸、癌症等,也都可發現RF因子的蹤跡。
值得注意的是,健康個體中也可能出現RF因子,甚至隨著年齡增長,檢出RF的比例也會隨之增加[2]。
▲ 在不同族群與疾病患者中檢測出RF陽性的比例[2]。
偽陽性訊號影響臨床診斷與治療決策
嗜異性抗體干擾hCG檢測值而誤診為惡性腫瘤
12位未懷孕的婦女,因持續檢出hCG[註]而被診斷為惡性絨毛膜癌,其中大部分患者接受了摘除手術與化療,但後續由不同檢測方式追蹤發現:最早在血清中驗出的hCG是由嗜異性抗體所造成的偽陽性結果[3]。
註: hCG為人類絨毛膜性腺激素,可用來檢測女性是否懷孕。有些癌症也會使血液中的hGC值偏高,臨床上採用ELISA方式進行血清檢驗。
嗜異性抗體干擾使心肌旋轉蛋白檢測值異常
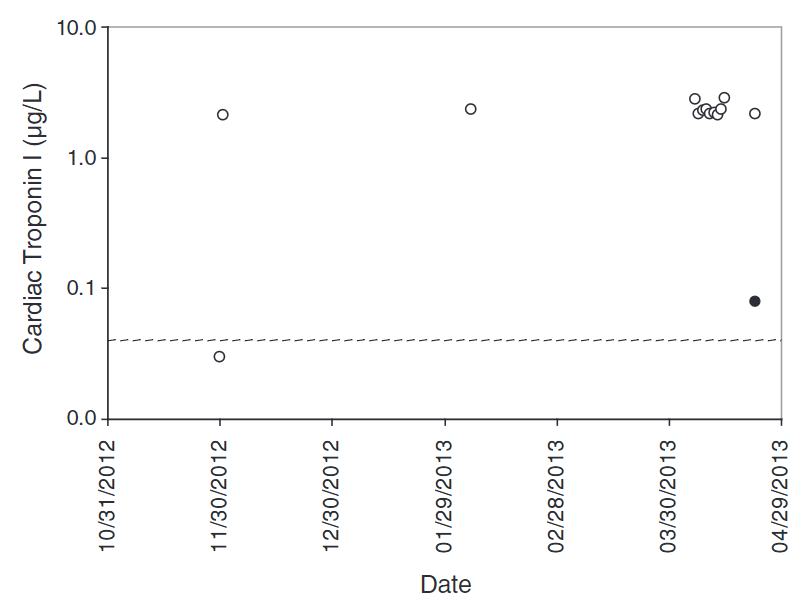
一名患有肥胖、高血壓、糖尿病等多種慢性病史的76歲女性,為裝置心律調節器而入院進行常規性檢驗,結果發現troponin I (cTnI) [註]異常超標 (檢測值2.13-2.85 µg/L;正常值 <0.04),但整合其他檢查結果並無發現心肌梗塞等相關徵兆。經後續追蹤檢測並採用嗜異性抗體阻斷劑(blocking buffer)重新分析,最終認為當時的troponin I檢測值是受到樣品中嗜異性抗體的干擾[4]。
註: Troponin I為心肌旋轉蛋白,是用來診斷心肌梗塞的重要指標,臨床上採用ELISA進行血清檢驗。
▲ 心肌旋轉蛋白 (cardio specific troponin I )檢測值。(○)為未經處理的血漿檢測值; (●)為嗜異性抗體阻斷劑 (blocking buffer)處理後的檢測值; 虛線為參考正常值。
新冠抗體血清檢測的偽陽性可能影響醫療策略
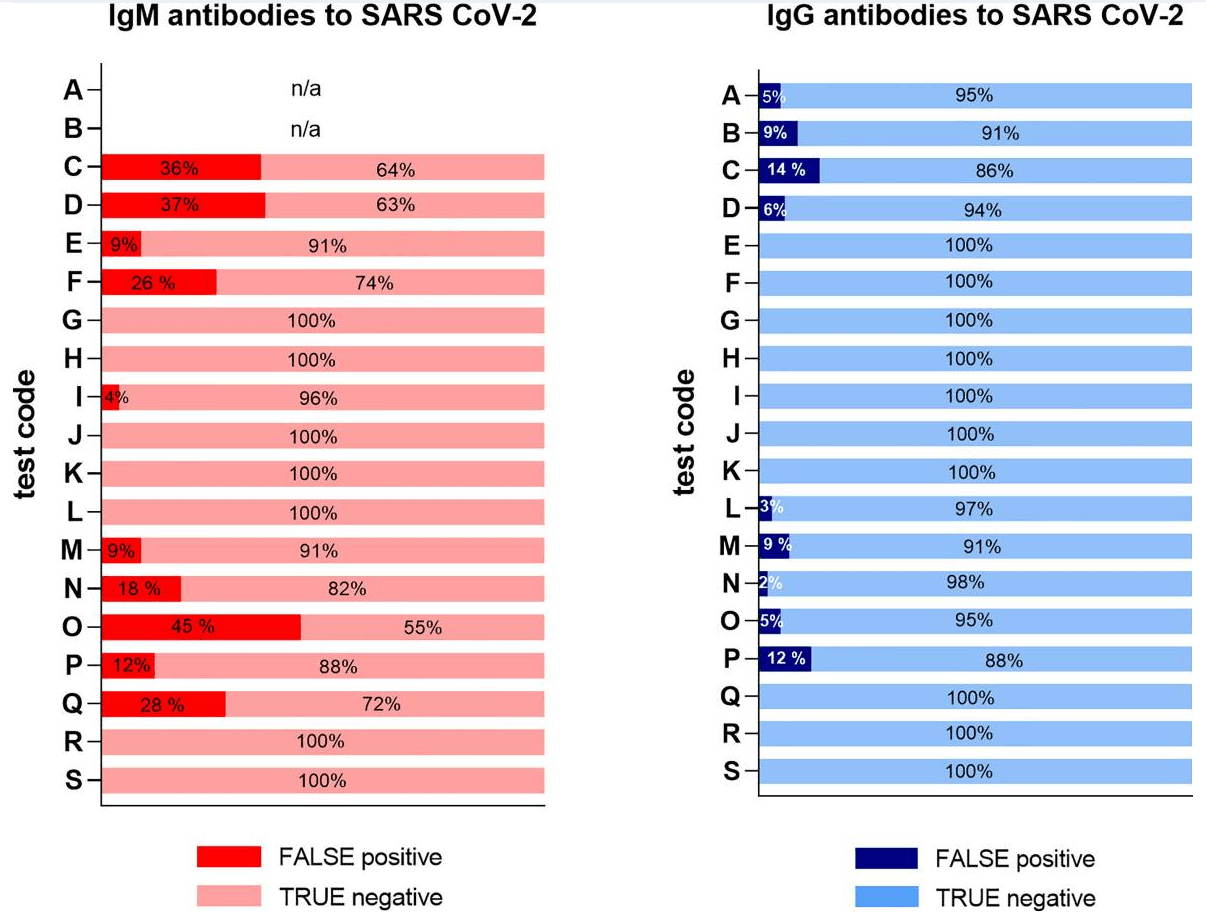
血清學研究在流行病學中相當重要,可協助了解病毒感染進程與人體免疫應答機制。在2019年新冠肺炎疫情爆發後,各國廠商紛紛投入快篩試劑的研發,協助研究人員快速掌握檢測數據。然而,針對特定族群的血清檢測,例如免疫相關疾病的患者,則容易因血清中的干擾因子比例高而造成偽陽性的結果。
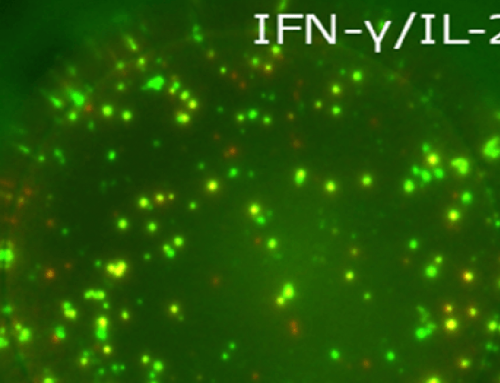
有研究顯示:取疫情爆發前慢性發炎疾病患者的血清檢測SARS-CoV-2抗體,在17家不同廠牌的檢驗試劑中,約有2~45% 的比例會出現偽陽性 (如圖)。
故極力呼籲,在研發或進行血清學相關的研究時,應將嗜異性抗體與RF因子可能造成的干擾納入考慮,因錯誤的檢測結果可能導致錯誤的醫療決策,甚至影響防疫策略[5]。
降低偽陽性的風險可提高臨床檢測的可信度
細胞因子(cytokine)是體內訊號傳遞的使者,除了調控免疫系統、也參與了許多重要的生理功能。分析細胞因子不只是學術研究探討各種分子機制的基礎,在臨床上也可做為疾病診斷或預後評估的重要生物指標。
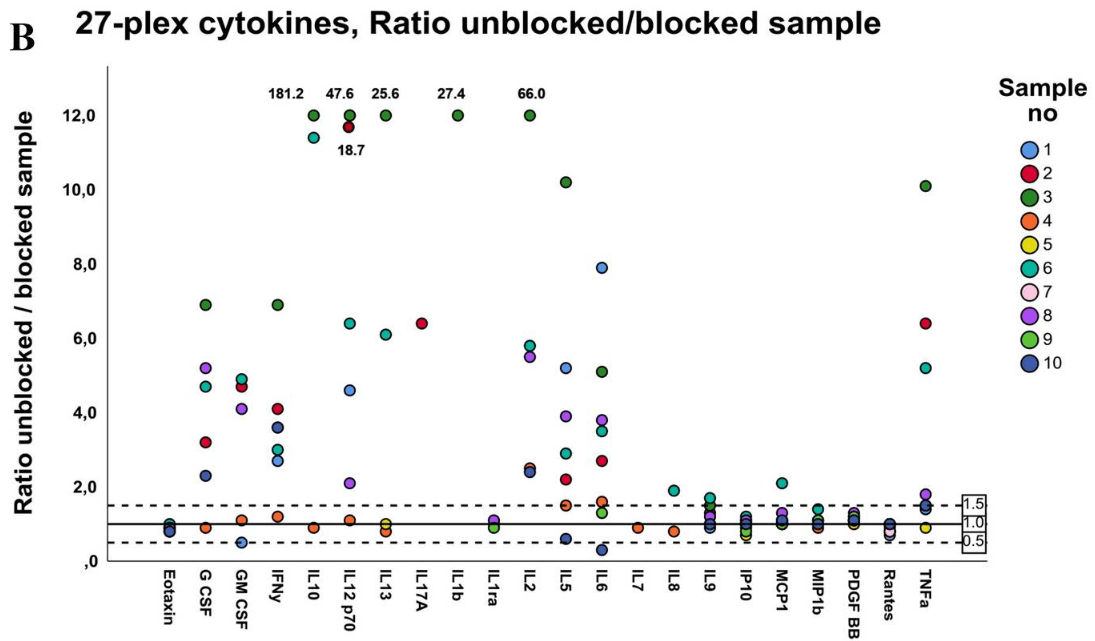
Gehin et al. 等人觀察一項關節炎世代研究中的樣品,討論RF因子在免疫分析試驗中可能對結果造成的影響。在多重因子試驗 (multiplex cytokine assay) 的結果顯示,70% 血清樣本會受到RF因子干擾,其中17/27的細胞因子觀察到顯著差異,包括常見的IFNγ、IL10、TNFα和IL-6等。
由於這些細胞因子在研究及臨床診斷上具重要意義,故作者在文中強調進行相關免疫試驗前,應做好適當的「防護措施」,避免檢體受RF因子或嗜異性抗體干擾而導致結果偏差[6]。
▲ 來自10位關節炎患者的血清樣品,透過多重因子試驗 (BioRed 27-plex cytokine assay)分析27種細胞因子的含量並比較有無添加阻斷劑的數值 (unblock/block)。比值 >1.5或 <0.5則判定為此檢體在檢驗中受干擾。
如何得知檢測樣品中是否存在干擾因子
- 檢體連續稀釋後,若檢測結果並非線性,則檢體中存在干擾因子。
- 使用不同技術方法分析檢體,確認結果的可信度。
- 使用不成對抗體免疫分析法 (unmatched ELISA)測試檢體。
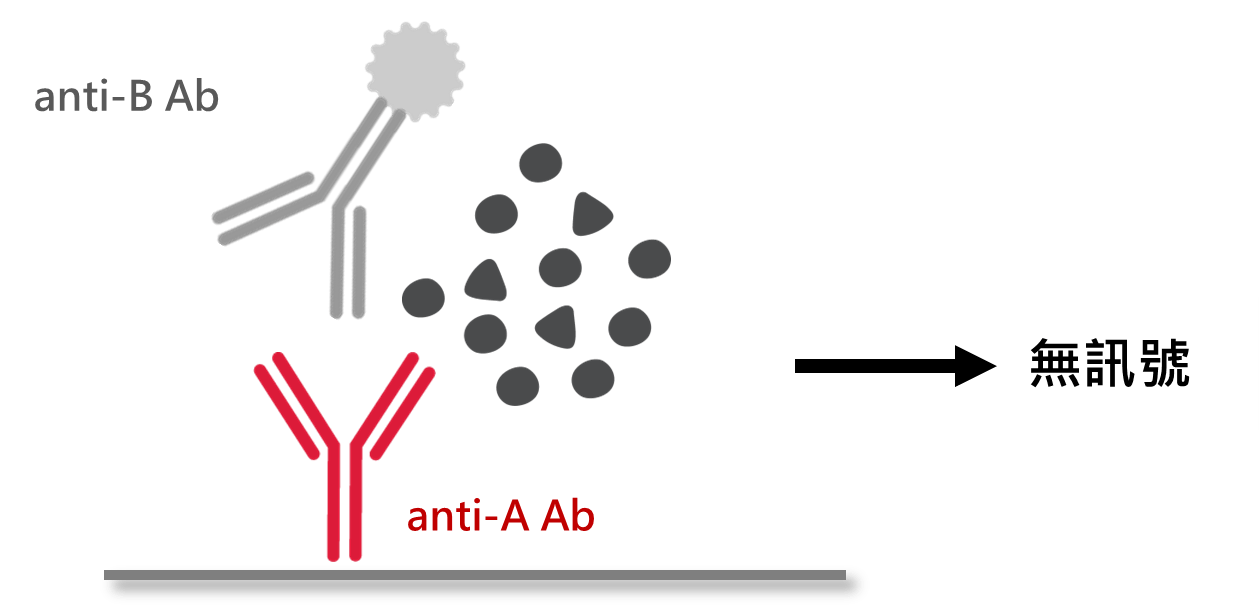
● 使用分別對應不同抗原的兩支抗體 (即不成對抗體)進行ELISA分析特定標的物的訊號。- 不存在干擾因子:沒有訊號產生
- 存在干擾因子:出現偽陽性訊號
▲ 不成對抗體分析法示意圖。
如何避免臨床檢體中干擾因子的影響 [7]
- 免疫干擾阻斷劑 (Blocking Buffer)
- 利用多種免疫球蛋白先行阻斷檢體中非特異性結合的抗體
- 檢體前處理 (pre-treatment):
- 萃取檢體中的目標分析物 (e.g., 凝膠層析法)
- 免疫萃取 (固相proteinA懸浮液)
- PEG 6000沉澱
- 將檢體加熱至70 ~ 90°C (以目標檢測物可耐高溫為前提)
- 採用不同物種來源的Capture Ab與Detection Ab
- 推薦! MABTECH ELISA PathRF 系列產品 👉🏻原廠說明
Mabtech ELISA PathRF系列產品有效降低干擾因子的影響
目前市面上的免疫分析套組大多附有阻斷劑 (blocking buffer)來減少嗜異性抗體的干擾。然而,嗜異性抗體並非單一形式存在,關於檢體中干擾因子的濃度或種類,目前仍缺乏有效的分析方法,故阻斷劑的抑制效果有限[1,6]。
Mabtech新推出的ELISA免疫分析套組系列產品 -- ELISA PathRF,重組蛋白合成的偵測抗體恆定區骨架 (Fc fragment)經過改造後,再搭配專用的RF-blocking 阻斷劑,可有效降低干擾因子所造成的偽陽性結果。
Mabtech ELISA PathRF效果經過RF陽性檢體驗證
不成對抗體ELISA檢測類風溼關節炎患者檢體
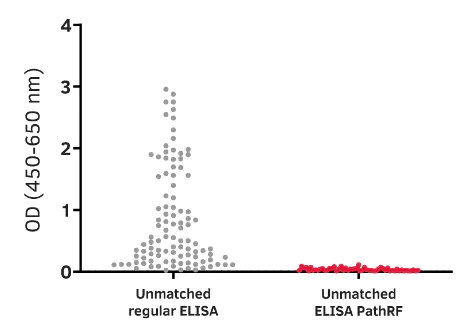
利用不成對抗體的ELISA可確認所獲得的訊號為真實或是偽陽性,因不成對抗體不能產生真正的訊號,若獲得訊號則表示檢體中存在干擾因子而導致偽陽性結果。
▲ 來自100位類風濕關節炎患者的血漿樣品,以不成對抗體ELISA分析,檢驗結果顯示:一般ELISA流程所得的偽陽性訊號頻率高;而使用ELISA PathRF 組別則幾乎沒有偵測到偽陽性的訊號。
Spike recovery assay效能驗證
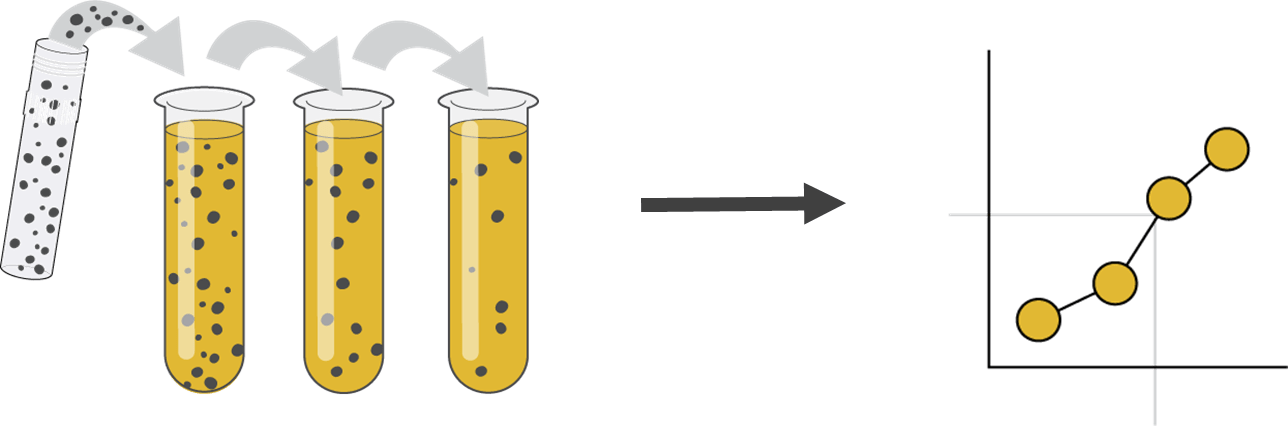
血漿中加入已知濃度的待測物,利用ELISA測定後分析測定量與添加量的比值以計算回收率,可評估產品的精准度 (precision)、線性 (linearity)與特異性 (specificity)。
▲ Spike recovery assay方法示意圖
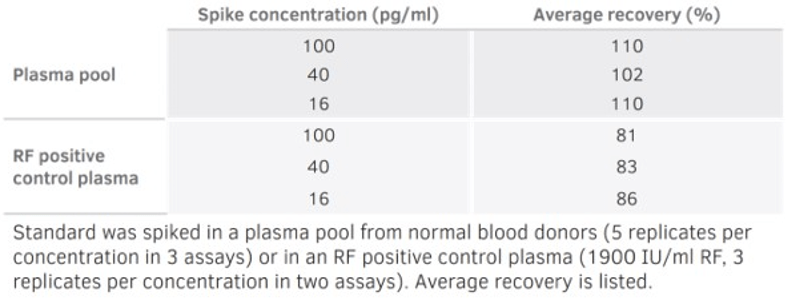
在健康貢獻者與RF陽性的血漿樣品中加入已知濃度的標準,利用ELISA PathRF試劑進行定量,最終健康來源組別回收率可達100%以上;RF陽性組別的回收率也可超過80%。其中,RF陽性組別的RF含量相當高,最終仍取得良好的分析結果。
▲ 健康來源組別與RF陽性組別中添加量與測定量的比率。
選擇MABTECH ELISA PathRF提升臨床診斷的正確性
ELISA在臨床醫學中有著重要的功能,可測定檢體中特定抗原的含量以進行後續的醫療評估。然而,血清學檢測可能因種種因素無法達到百分百的準確,但撇除外在的干擾,實驗人員可透過試劑的選擇,大大降低檢體內干擾因子的影響,進而提升數據的準確性與可信度,也為醫護人員與患者帶來更多福祉。
MABTECH ELISA PathRF 產品列表
參考文獻
- Bolstad, Nils, David J. Warren, and Kjell Nustad. "Heterophilic antibody interference in immunometric assays." Best practice & research Clinical endocrinology & metabolism 27.5 (2013): 647-661.
- Ingegnoli, Francesca, Roberto Castelli, and Roberta Gualtierotti. "Rheumatoid factors: clinical applications." Disease markers 35.6 (2013): 727-734.
- Rotmensch, Sigi, and Laurence A. Cole. "False diagnosis and needless therapy of presumed malignant disease in women with false-positive human chorionic gonadotropin concentrations." The Lancet 355.9205 (2000): 712-715.
- Lippi, Giuseppe, et al. "Interference from heterophilic antibodies in troponin testing. Case report and systematic review of the literature." Clinica Chimica Acta 426 (2013): 79-84.
- Kharlamova, Nastya, et al. "False positive results in SARS-CoV-2 serological tests for samples from patients with chronic inflammatory diseases." Frontiers in immunology (2021): 1365.
- Gehin, Johanna E., et al. "Rheumatoid factor and falsely elevated results in commercial immunoassays: data from an early arthritis cohort." Rheumatology international 41.9 (2021): 1657-1665.
- Tate, J., & Ward, G. (2004). Interferences in immunoassay. The clinical biochemist reviews, 25(2), 105.